Medicamentos genéricos: ¿en ayunas?
¿En ayunas o con las comidas? Es una de las preguntas más frecuentes que se hacen los pacientes cuando inician un tratamiento con medicamentos que se administran por vía oral.
Los propios pacientes tienen la percepción de que la presencia o ausencia de alimentos en el estómago puede condicionar la respuesta clínica de los tratamientos farmacológicos.
Aunque son bien conocidas las ventajas que ofrece la vía oral para la administración de medicamentos, especialmente en tratamientos crónicos, la variabilidad en la biodisponibilidad es una de sus principaleslimitaciones. Conocer la biodisponibilidad es uno de los objetivos a alcanzar durante la fase I en el desarrollo clínico de los medicamentos innovadores y su conocimiento es esencial para seleccionar la vía de administración y para establecer las pautas de dosificación.
Los parámetros farmacocinéticos, Cmax (concentración sérica máxima), tmax (tiempo al que se alcanza Cmax) y el AUC (área bajo la curva concentración sérica-tiempo) permiten el cálculo de la biodisponibilidad oral. Estos mismos parámetros son necesarios para establecer la bioequivalencia, en velocidad y magnitud, en relación con una formulación de referencia en el desarrollo de los medicamentos genéricos. La variabilidad en la biodisponibilidad afecta tanto a los medicamentos innovadores como a los medicamentos genéricos y tiene especial importancia con fármacos oncológicos, antiarrítmicos y algunos psicofármacos.
La mejor medicina puede ver comprometida la eficacia y/o seguridad en el paciente si ignoramos el efecto que pueden provocar los alimentos
Son numerosos los factores que pueden modificar la biodisponibilidad por vía oral y algunos están relacionados con la anatomía, la fisiología y la patología del tracto gastrointestinal (pH gástrico, tiempo de vaciado gástrico y motilidad intestinal, volumen y composición del fluido intestinal, flujo esplácnico, cirugía, estreñimiento crónico, etc.). Pero la cantidad de fármaco que alcanza la circulación general no está sólo en función de la cantidad absorbida por el epitelio digestivo (y, por tanto, de la dosis administrada) sino también de otros procesos de eliminación presistémica que pueden reducir la biodisponibilidad de medicamentos aunque se absorban de forma completa en el tracto gastrointestinal: degradación en la luz intestinal, metabolismo en los enterocitos y captación hepática de primer paso. El metabolismo por efecto de “primer-paso” afecta a la biodisponibilidad de muchos medicamentos orales. En los enterocitos se expresan diversas isoenzimas del CYP450, principalmente CYP3A y CYP2C9, capaces de biotransformar numerosos fármacos, como midazolam, verapamilo o tacrolimus, entre otros.
Biodisponibilidad
Los alimentos y sus interacciones con fármacos pueden modificar la biodisponibilidad, conocido como food effect bioavailability, cuyas consecuencias son, en principio, impredecibles, dependiendo de la relación farmacocinética/farmacodinamia (pK/pD).
No todos los alimentos producen el mismo efecto ni todos los medicamentos ven afectada su biodisponibilidad, ni cuando esto ocurre la modificación se produce en el mismo sentido o con la misma intensidad. Así, conocemos que la presencia de alimentos incrementa la biodisponibilidad del nifedipino de liberación prolongada más del 30 por ciento, lo cual se refleja en un claro incremento de su efecto hipotensor. Por el contrario, la presencia de alimentos en el estómago no afecta a la biodisponibilidad del metoprolol. La composición nutricional de la ingesta (contenido en grasas, poder calórico, contenido proteico, etc.) puede afectar a la exposición sistémica. Así, el lapatinib, un inhibidor de la tirosina quinasa indicado en el tratamiento del cáncer de mama, en presencia de alimentos grasos, experimenta un incremento en el valor de AUC superior al 200 por ciento en relación con el valor obtenido en ayunas.
Las propiedades fisicoquímicas y biofarmacéuticas deben ser tomadas en consideración para la predicción del efecto delos alimentos en la biodisponibilidad, que incluyen métodos in vitro e in vivo.
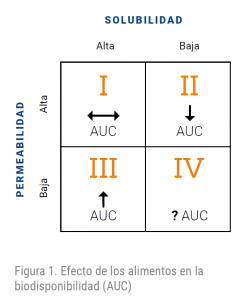
El Sistema de Clasificación Biofarmacéutica (BCS, por sus siglas en inglés) agrupa los fármacos según los valores de solubilidad y permeabilidad en cuatro clases (I-IV), ambos directamente relacionados con el proceso de absorción y diferentemente afectados por la presencia de alimentos en el tracto gastrointestinal, cuyo efecto sobre el grado de exposición a los fármacos (AUC) para las clases I-IV se recoge en la figura 1.
Aunque no existen dudas sobre las posibilidades de aplicación del BCS en estudios de biodisponibilidad y bioequivalencia, al tratarse de un método in vitro tiene algunas limitaciones. Así, la predicción para fármacos de la clase II y IV es todavía un desafío para la investigación farmacéutica. A pesar de ello, dada su innegable utilidad, la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) adoptó en 2020 la Guía ICH M9 basada en el Sistema de Clasificación Biofarmacéutica.
Machine learning
Los modelos biofarmacéuticos con base fisiológica (PBBM, por sus siglas en inglés) han sido aplicados a la predicción del efecto de los alimentos utilizando simulación in silico con paquetes informáticos como GastroPlus®, SimCyp®, PK-Sim® y STELLA®. Este cálculo de la bioequivalencia virtual ha sido aplicado con éxito incluso a fármacos escasamente solubles incluidos en las clases II y IV de la BCS. Su aplicación reduce tiempo y costes en la producción farmacéutica y evita la exposición de voluntarios sanos a los fármacos. La aplicación de esta metodología figura entre las prioridades de investigación en las Generic Drug User Fee Amendments (GDUFA) desde 2018.
El uso de técnicas de machine learning ha demostrado ser de utilidad para numerosas aplicaciones, entre ellas la investigación biomédica. En los últimos años, se ha dado un impulso a la aplicación de las redes neuronales artificiales (ANN, por sus siglas en inglés) en el desarrollo farmacológico, incluyendo la prediccióndel food effect. Experiencias con modelos predictivos utilizando algoritmos y modelos computacionales, como máquinas de vectores soporte y redes neuronales artificiales, han conseguido mayor precisión que aplicando el BCS. El documento de la EMA, Regulatory Science 2025, ya incorpora el aprendizaje automático y la inteligencia artificial en la investigación farmacéutica.
La mayoría de los estudios de bioequivalencia se realizan con el paciente en ayunas por ser la condición más sensible para detectar la potencial diferencia entre formulaciones. Los estudios clínicos destinados a conocer el efecto de los alimentos en la biodisponibilidad se han intensificado en los últimos años. En enero de 2022, la base de datos Clinical- Trials.gov promovida por los Institutos de Salud de Estados Unidos (NIH, por sus siglas en inglés) incluía más de dos mil estudios clínicos destinados a conocerel efecto de los alimentos en la biodisponibilidad.
Medicamentos Genéricos
La EMA ha establecido las siguientes normativas aplicables a los estudios sobre el food effect para la autorización demedicamentos genéricos: investigación de bioequivalencia, investigación de interacciones, investigación farmacocinética y evaluación clínica en las formulaciones de liberación modificada.
En 2013, la EMA inicia el desarrollo del programa “Produc-Specific Bioequivalence Guidelines”, una importante iniciativa para el desarrollo de los medicamentos genéricos. En enero de 2022, se habían incorporado al programa guías de bioequivalencia de más de 70 fármacos que contienen información relevante para la autorización por procedimientos centralizados en la Unión Europea.
Estas guías están dirigidas principalmente a medicamentos genéricos para el tratamiento del cáncer, enfermedades degenerativas y síndrome de inmunodeficiencia adquirida. En ellas se incluye la clase del BCS a la que pertenece cada fármaco, su solubilidad, el tipo de diseño del estudio de bioequivalencia, los parámetros farmacocinéticos requeridos, así como la necesidad, o no, de realizar estudios clínicos sobre el efecto de los alimentos en la biodisponibilidad.
En 2019, la agencia estadounidense del medicamento (FDA, por sus siglas en inglés) publicó los borradores de dos nuevas guías: 1- Bioavailability Studies Submitted in NDAs or INDs – General considerations,y 2- Assessing the Effects of Food on Drug in INDs and NDAs – Clinical Pharmacology Considerations. En palabras del entonces Comisionado de la FDA, Scott Gottlib, estas guías incorporan los avances que se hanproducido en el diseño y desarrollo de los estudios sobre el efecto de los alimentos en la biodisponibilidad (AUC), en la variabilidad de la exposición sistémica a los fármacos y sobre las posibles diferencias en el efecto de alimentos con distintos contenidos en grasa o poder calórico.
El desarrollo de nuevos tratamientos orales anticipa un futuro prometedor para los medicamentos genéricos
Es responsabilidad de los profesionales sanitarios informar a los pacientes de las precauciones necesarias que deben adoptar al iniciar un tratamiento por vía oral para obtener los mejores resultados clínicos. La biodisponibilidad debe ser controlada. El paciente está esperando.
El desarrollo de nuevos tratamientos orales frente al cáncer, diabetes, esclerosis múltiple y más recientemente frente a la COVID-19 anticipa un futuro prometedor para los medicamentos genéricos.
Hace 2.500 años, Hipócrates de Cos citaba “que el alimento sea tu mayor medicina y tu mejor medicina sea tu alimento”. Hoy sabemos que incluso la mejor medicina puede ver comprometida su eficacia y/o seguridad en el paciente si ignoramos el efecto que pueden provocar los alimentos.
Alfonso Domínguez-Gil Hurlé
Catedrático Emérito de la
Universidad de Salamanca